Contents
A importância da calibração em uma farmacêutica
Para a produção, distribuição e distribuição de medicamentos para a indústria farmacêutica precisa de vários processos normativos. Durante toda a cadeia produtiva são utilizados instrumentos para medir, registrar e controlar variáveis de processo. E é de extrema importância garantir a confiabilidade dos instrumentos utilizados no processo industrial e laboratorial. Para isso é usado o processo de exclusão dos instrumentos veja abaixo os principais pontos para organizar e implementar e executar a operação dentro de uma indústria farmacêutica.
Planejamento
- Identificação dos Instrumentos : Listar todos os instrumentos que precisam de permanência.
- Definição dos Padrões de Referência : Escolha padrões de referência protegidos com uma solução superior aos instrumentos a serem calibrados.
- Elaboração do Cronograma : Estabeleça um cronograma de funcionamento regular, geralmente baseado na criticidade do instrumento e nos requisitos regulamentares.
Preparação
- Documentação : Preparar todos os documentos necessários, incluindo procedimentos operacionais padrão (SOPs) e registros de ocorrências.
- Ambiente de Calibração : Garanta que o ambiente de isolamento seja controlado em termos de temperatura, umidade e ausência de interferências.
Execução
- Verificação Inicial : Verifique o estado do instrumento e registre suas condições iniciais.
- Medições : Compare as leituras do instrumento com as do padrão de referência. Faça várias variações para garantir precisão e confiabilidade.
- Ajustes : Se necessário, ajuste o instrumento para que suas leituras correspondam ao padrão de referência.
- Repetição : Repita a profundidade após o ajuste para confirmar a precisão do instrumento.

https://www.dicasdeinstrumentacao.com/procedimento-de-calibracao-de-sensores-de-pressao-diferencial/
- Documentação
- Registro de Calibração : Documente todas as precisão, ajustes e condições do teste. Inclui dados como:
- Identificação do instrumento
- Dados da confiança
- Resultados das decisões antes e após os ajustes
- Identificação do padrão de referência utilizado
- Nome do técnico responsável
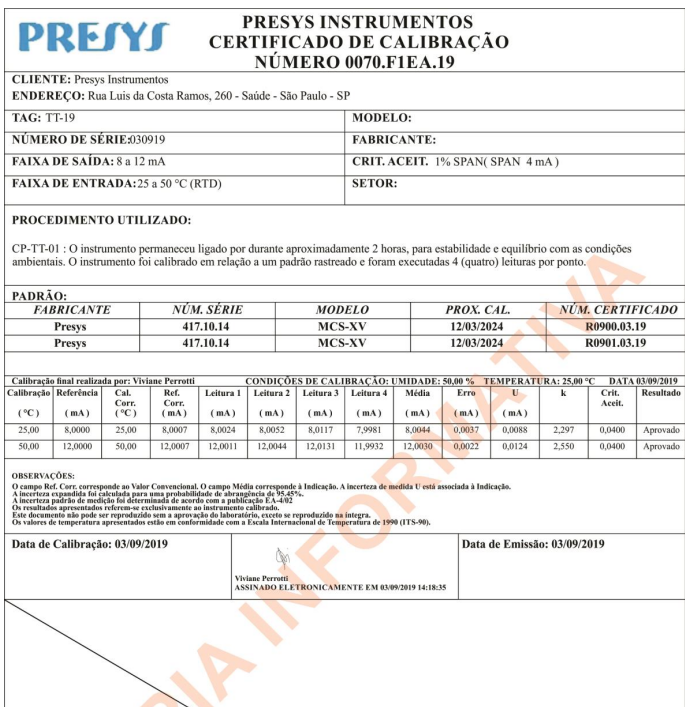
- Certificado de Calibração : Emita um certificado que inclui todos os detalhes da deficiência, sendo este um documento importante para auditorias e conformidade regulatória.
Análise e Ação Corretiva
- Análise dos Resultados : Avaliar os resultados da descoberta para identificar tendências ou desvios que possam indicar problemas futuros.
- Ação Corretiva : Se um instrumento não puder ser calibrado corretamente, ele deverá ser reparado ou substituído. Também é importante verificar o impacto das especificações incorretas feitas anteriormente.
Revisão e Aprovação
- Revisão dos Registros : Verifique e aprove todos os registros e certificados de ocorrência.
- Aprovação : A aprovação final deve ser feita por uma pessoa qualificada, geralmente um analista de metrologia, supervisor ou gerente de qualidade.
Boas Práticas de Calibração
- Calibração Rastreável ou RBC : Utilize padrões de referência que sejam rastreáveis a organismos nacionais ou internacionais, como NIST (Instituto Nacional de Padrões e Tecnologia) ou INMETRO (Instituto Nacional de Metrologia, Qualidade e Tecnologia).
- Intervencionismo ou verificação contínua : Intervenha imediatamente se um instrumento apresentando leituras fora dos limites aceitáveis.
- Documentação : Mantenha registros detalhados e organizados de todas as calibrações para fins de auditoria e conformidade. A exemplos do PMC – Plano Mestre de Calibração.
- Capacitação Contínua : Certifique-se de que os técnicos de treinamento recebam treinamento contínuo e tenham atualizações sobre as melhores práticas e normas vigentes. Dentre eles:
- NBR ISO 17025:2017 Requisitos gerais para a competência elaboratória de ensaio e segurança
- ANSI – ISA 5.1 – Identificação dos Instrumentos
- RDC 658/2022 – Boas Práticas de Fabricação de Medicamentos.
Conclusão
A intervenção de instrumentos na indústria farmacêutica é um processo específico que exige planejamento cuidadoso, execução precisa e especificações detalhadas. Este processo é essencial para garantir a precisão da precisão, a qualidade dos produtos e a conformidade com as regulamentações. Profissionais bem treinados e procedimentos robustos são cruciais para o sucesso das atividades de confiança e, consequentemente, para a integridade dos produtos farmacêuticos.
Se você tem interesse sobre o sobre indústria farmacêutica, acesse nosso site: industriafarma.com e veja também o artigo: https://industriafarma.com/reprovei-metade-do-lote-novo-de-vidrarias/






[…] Veja mais artigos como esse: https://industriafarma.com/como-fazer-a-calibracao-de-instrumentos-em-uma-industria-farmaceutica/ […]